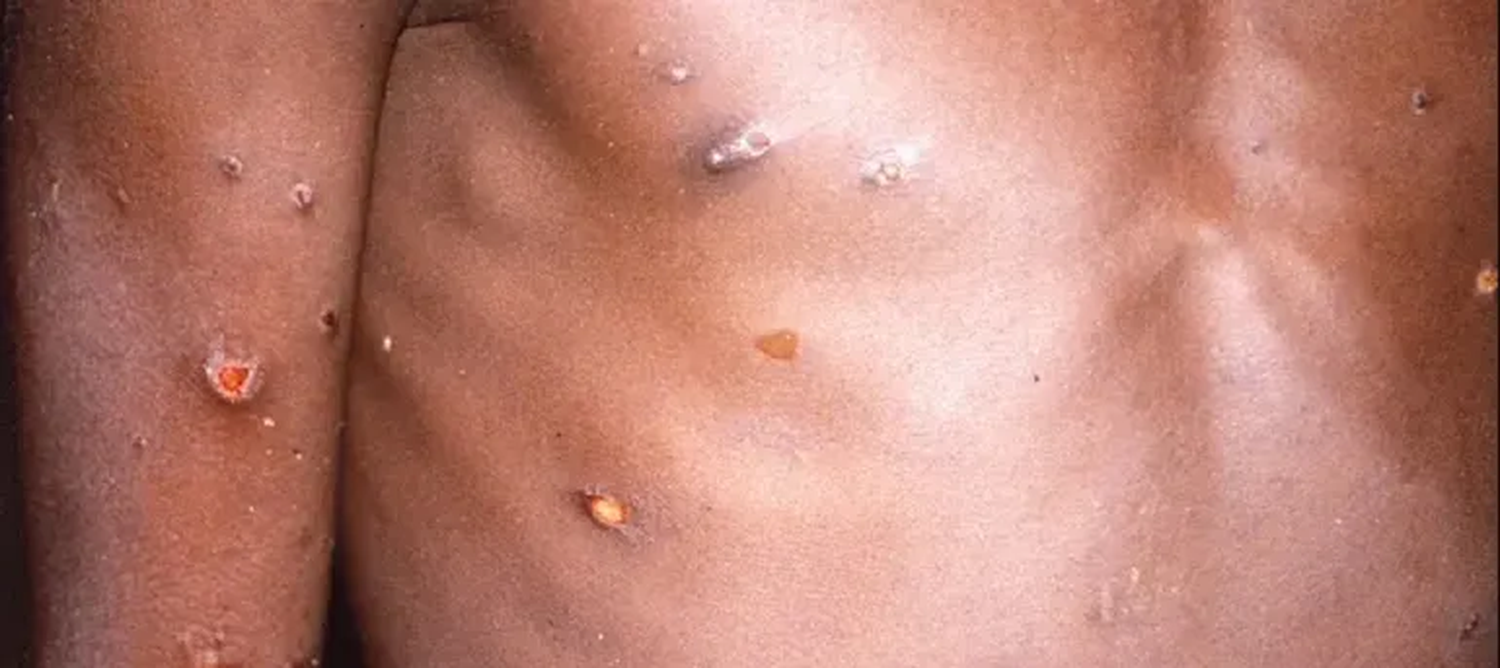
Viruela del mono: ¿qué aprendieron los médicos en el Reino Unido a lo largo de los años?
Por Ramiro Heredia (Doctor Clínico MN 117882)
Se publicó el 24 de mayo en The Lancet, la prestigiosa revista médica británica, Características clínicas y manejo de la viruela del mono humana: un estudio observacional retrospectivo en el Reino Unido (1). Un grupo de investigadores británicos analizó los 7 casos tratados en la región desde agosto de 2018 a septiembre de 2021, es decir, antes de las series de casos actuales que despertaron el interés de la comunidad científica.
La viruela del mono en humanos
Los casos de viruela del mono humana son raros fuera de África Occidental y Central. Excepto un gran brote en los Estados Unidos asociado a roedores en el 2003 (47 infectados, sin casos confirmados de transmisión persona a persona), la transmisión de la viruela del mono siempre estuvo limitada a regiones de África.
La mortalidad es del 1-10%. El virus del clado o subtipo Occidental, que es el responsable de los casos actuales fuera de África, está asociado a una mortalidad del 3%, y es el responsable de los casos actuales.
Las poblaciones más vulnerables y con mayor riesgo de morir son los niños y las personas que viven con HIV.
Hay pocos hay medicamentos específicos con licencia. Dos drogas orales fueron aprobadas para la viruela: brincidofovir y tecovirimat. Este último, en primates no humanos, disminuyó la muerte por viruela, así como la viremia y la eliminación del virus en secreciones de vía aérea superior. �0stas demostraron también ser eficaces contra la viruela del mono en animales (pero no se probó su eficacia en humanos).
Clásicamente se considera que las personas con viruela del mono contagian hasta que las lesiones en piel se vuelven costras.
La transmisión de persona a persona se empezó a considerar como una amenaza para la salud pública en 2018, tras los casos reportados en Nigeria.
En los entornos habituales en que se presentan los casos (países en desarrollo, con sistemas de salud con recursos limitados), raramente se pudo tomar muestras para realizar pruebas moleculares repetidas en el tiempo, por lo cual la dinámica viral no es del todo clara.
El objetivo de este grupo de investigadores británicos fue describir el curso a lo largo del tiempo de la viruela del mono (es decir, el tiempo de incubación, evolución de los síntomas y complicaciones, así como la eliminación viral y posibilidad de diseminación, tratamientos usados y sus efectos adversos) en un país de altos ingresos.
Esto es muy importante, ya que muchas enfermedades endémicas de países de bajos ingresos, como por ejemplo el �0bola en África, tienen una mortalidad en su país de origen y una muy distinta cuando son tratados en un país desarrollado (2).
El método: ¿Cómo se hizo este estudio?
Se realizó un estudio observacional retrospectivo de una serie de casos. Analizaron caso por caso, y trataron de agrupar los resultados y sacar conclusiones.
Reportaron las características clínicas, los hallazgos virales a lo largo de tiempo (desde y hasta cuando se elimina el virus, y en que muestras), así como a la respuesta a los tratamientos «fuera de etiqueta» (aquellos no aprobados aún para un uso dado), en 7 pacientes con diagnóstico de viruela del mono en el Reino Unido, desde 2018 a 2021, en 2 centros médicos especializados en enfermedades Infecciosas de alto riesgo.
Se tomaron muestras de vía aérea superior, sangre, orina y de las lesiones presentes cada 48-72 horas, hasta tener 2 resultados negativos. La técnica que se uso fue PCR. El criterio de alta hospitalaria de los pacientes fue este más resolución de las lesiones en piel y mucosas.
Hallazgos: ¿Qué observaron?
Se analizaron 7 pacientes: 4 hombres, 3 mujeres. Todos eran jóvenes, y sanos (entre 30-40 años, salvó un niño menor de 2). Ninguno estaba vacunado contra la viruela. 4 eran casos «importados» de países endémicos. 3 se contagiaron en el Reino Unido: uno era un trabajador de salud que se contagió en el hospital, y otro de estos era conviviente de otros casos.
La mayoría tuvo síntomas leves a moderados. A todos se los internó con el objetivo de controlar las infecciones, no por la gravedad de su enfermedad.
Ninguno tuvo las complicaciones graves conocidas de la viruela del mono: neumonitis y sepsis bacteriana.
Todos tuvieron lesiones en piel que fueron positivas por PCR para el virus, junto con hisopados de vía aérea superior, también positivos.
6 tuvieron ADN detectable en sangre (es decir, viremia), y 4 tuvieron PCR positiva en orina.
Estos fueron los puntos clínicos y virológicos destacados:
Se detectó el virus en la sangre (viremia) de los pacientes durante un tiempo prolongado.
Detección prolongada de ADN viral en hisopados de vía aérea superior, incluso más allá de resueltas las lesiones en piel.
5 pacientes requirieron más de 3 semanas de aislamiento (22-39 días), por seguir dando positivo en las PCR de hisopados de vía aérea superir.
Respecto al tratamiento, estos fueron los resultados:
3 pacientes recibieron brincidofovir, y los 3 tuvieron elevación de las transaminasas (inflamación del hígado), lo que llevo a suspender el tratamiento. Este demostró grandes beneficios clínicos. 1 paciente recibió tecovirimat, sin eventos adversos y con una duración menor de la eliminación viral y de la enfermedad (10 días), en comparación con los otros 6 pacientes.
¿Cómo se interpreta esto?
El virus de la viruela del mono en humanos es un desafío para la salud pública global, ya que es capaz de cruzar las fronteras, y de mantener su transmisión fuera de áreas endémicas.
La eliminación prolongada de ADN viral en vías aéreas superiores, después de la resolución de las lesiones en piel, desafía las pautas actuales de control y prevención de infecciones.
Se requieren estudios prospectivos (es decir, en los que los investigadores intervengan) para evaluar los antivirales disponibles en esta enfermedad.
Puntos Clave de la investigación
Se publicó en The Lancet una serie de 7 casos de viruela del mono en el Reino Unido, hasta 2021. Todos eran paciente jóvenes, sanos y no vacunados contra la viruela. Todos tuvieron un curso clínico benigno. Se probaron 2 antivirales: solo el tecovirimat, probado en un solo paciente, mostró acortar el tiempo de eliminación viral y una evolución clínica más leve.
6 de los 7 pacientes tuvieron viremia, y algunos pacientes eliminaron ADN viral en vías aéreas superiores más allá de los 21 días de aislamiento recomendados, y una vez resueltas las lesiones cutáneas (22-39 días), que es un criterio clásico de alta, ya que se consideraba que a partir de ahí el individuo no contagiaba más.
Referencias
(1). https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(22)00228-6/fulltext
(2). https://www.uptodate.com/contents/clinical-manifestations-and-diagnosis-of-ebola-virus-disease?csi=878dcdc3-f389-49de-a4be-3d0c477c81bc&source=contentShare
Autor: Ramiro Heredia (@ramiroherediaok)
Fuente: https://infomed.com.ar/